急性肾损伤(AKI)是住院患者中常见的疾病,AKI 的治疗管理要求对水、电解质平衡有深入了解以及在急性期能够正确应用肾脏替代治疗(RRT)。旨在为肾脏病专业培训人员提供专业核心知识的 AKI 2018 核心教程发表于近期的 AJKD 杂志上。
教程回顾了有关 AKI 诊断和常规处理的主要原则:一旦出现 AKI,应该立即寻找病因,特别警惕有无可逆性因素存在。防治 AKI 的措施包括最佳的容量状态以及避免肾毒性药物的应用。对于大多数患者,晶体液补充优于胶体液,另外应当避免羟乙基淀粉应用。
在 AKI 病程中,容量过负荷同不良预后相关,因此需要注意整体的液体平衡。目前尚没有获批的 AKI 靶向治疗药物。合并有 AKI 的危重患者行 RRT 的最佳时机仍不清楚,是值得探索的领域。另外,近期的研究显示 AKI 并不是个「自限」的过程,其同增加慢性肾脏病(CKD)风险、后续的 AKI 以及远期的死亡率密切相关。
一、AKI 的诊断和评估
AKI 表现为肾功能急剧下降后肌酐、尿素氮以及未测定代谢废物在体内的蓄积。近年来,「损伤」已经代替了「衰竭」以强调疾病的连续性,因为即使适度的肾功能下降也会导致更差的结局。大约 5%~10% 的住院患者以及高达 60% 的入住 ICU 的患者会出现 AKI。当 AKI 发生时,关键的第一步是评估病因,尤其注意有无可逆因素。
二、AKI 的定义
由于之前的研究具有明显的的异质性,在过去的 10 年中,相关专业人士一直努力探索有关 AKI 定义的共识,尤其是用于流行病学研究以及临床试验。2012 年,KDIGO 工作组组合了之前 AKI 定义的相关内容(表 1)。分期基于尿量和血肌酐水平考虑,如果尿量和血肌酐变化并不相符,建议考虑最高分期。应该注意,考虑到危重患者较高的液体摄入量,不管血肌酐是否发生改变,单以尿量的变化判定发生 AKI 的患者,通常有液体过负荷的风险。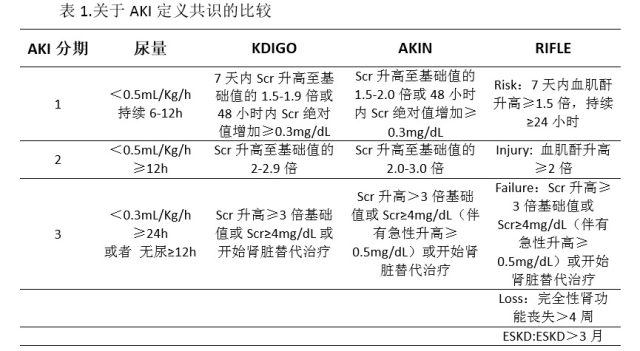
急性损伤背景下的肾功能评估 
目前所用的 eGFR 公式(Cockcroft-Gault,MDRD 以及 CKD-EPI)在血肌酐不稳定的情况下,不能使用。此外,由于血肌酐滞后于肾功能的急性变化,当前 AKI 的分期可能并没有反映当前的肾功能。急性病期间血肌酐生成的减少、肌肉减少症(常伴发于长期的疾病)、以及容量超负荷时血肌酐的稀释,使肾功能的评估进一步复杂化。
虽然开发床旁实时测量 GFR 的工具比较吸引人,但目前临床仍没有这样的检测工具。肾小管损伤生物标记物包括 NGAL,KIM-1,IL-18,L-FABP 等,今后 AKI 定义可能会包括生物标记物。反映肾脏应激的生物标记物包括 TIMP-2,IGFBP-7,最近已获美国 FDA 批准,用于鉴别在随后的 12~24 小时内会发展为 KDIGO 2~3 期 AKI 的高风险患者。
三、AKI 病因及常规治疗
1.AKI 病因评估
对于符合 AKI 诊断的患者,应尽快寻找病因(表 2),细致的病史采集、病例回顾、体格检查是工作的基本原则。对于所有 AKI 患者均需用生命体征和体格检查来仔细评估血流动力学以及容量状态。

2.AKI 治疗概述
对于有 AKI 风险及已发生 AKI 的患者,应该通过血肌酐以及尿量严密监测肾功能。避免肾毒性药物应用,调整药物剂量,尤其是对于 AKI 2 期或 3 期的患者(框 2)。例如,AKI 患者应用钆剂,可能引起肾源性系统性纤维化,虽然发生率较低,仍建议仔细评估应用钆剂的风险及获益。联用哌拉西林他唑巴坦可能会增加万古霉素肾毒性,具体机制尚不清楚。
(1)血流动力学支持:液体管理和血压靶标
对于 AKI 患者的血流动力学管理意义重大,尤其是有休克的患者中。在正常生理情况下,肾脏能够调节自身血流,而在 AKI 情况下,这些机制均被破坏。
(2)静脉液体复苏
a. 胶体液和晶体液
胶体液,例如白蛋白、羟乙基淀粉和明胶,依赖于胶体渗透压梯度选择性扩张血管内容量,而晶体液平衡血管内和血管外间隙,炎症状态会增加患者血管通透性,从而减少应用胶体液的获益。白蛋白(以及其他的胶体液)应该避免在脑外伤患者中使用,因为可增加死亡风险。相关研究提示使用胶体的关键之处是决定最佳给药时机,目前,尚无资料支持容量复苏时常规使用胶体液。
b. 生理平衡盐溶液和生理盐水
等渗生理盐水同细胞外液相比,有更高的氯含量(154 mmol/L VS 约 110 mmol/L),接受生理盐水患者有高氯性酸中毒的风险,动物试验中,高氯增加肾血管阻力,增加肾素活性以及降低 GFR。在健康志愿者中应用生理盐水和生理平衡盐溶液对比,生理盐水增加血管外容量,减低肾皮质灌注。关于高氯液是否增加 AKI 风险仍存在有不同的研究结果。
(3)血压管理
血压靶标需要考虑发病前血压,需要权衡血管收缩导致肾灌注增加以及其他器官低灌注之间的利弊关系。
(4)AKI 的其他治疗:利尿剂,营养和预后
a. 利尿剂:KDIGO 不推荐应用利尿剂治疗 AKI,除非有容量超负荷的情况存在。
b. 营养和血糖控制:关于 AKI 血糖的管理,KDIGO 指南中推荐危重患者血糖控制于 110~149 mg/dL 之间,但此血糖范围从未在随机临床试验中正式评估。部分研究发现,严格血糖控制同更高的死亡率相关,并且增加了低血糖发生风险。考虑到肾脏在胰岛素代谢以及血糖排泄中的作用,AKI 患者出现严重低血糖风险增加。然而,高血糖同样增加各种临床病症的发病率和死亡率,也应该避免。
(5)AKI 的药物治疗
目前尚没有阻止或治疗 AKI 的有效药物治疗(框 3)。由于 AKI 疾病本身的异质性,以单一的疗法来治疗所有的 AKI 难以实现。另外,AKI 损害通常发生于 AKI 可检测之前,因此疾病发生之前难以早期干预。早期发现 AKI 以及应用在多种病理过程中均能起到作用的药物治疗有望成功。
(6)严重 AKI 的管理,包括肾脏替代治疗
AKI 患者会出现高钾,代谢性酸中毒,容量过负荷和/或尿毒症症状,高钾的药物治疗(见表 3)。尽管有这些临时处理措施,严重的 AKI 仍然需要肾脏替代治疗,肾脏替代的最佳时机仍是研究活跃的领域。由于相关临床试验的研究方法差异以及研究人群的选择偏倚,是否早期肾脏替代治疗获益更多,以及何种人群需要早期肾脏替代治疗,这些问题尚无定论。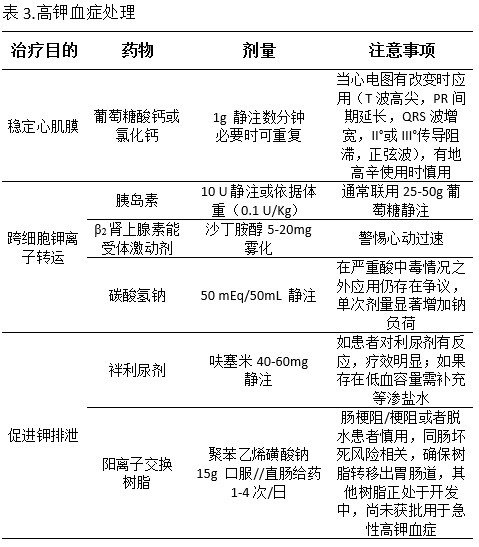
肾脏替代治疗处方:包括模式和剂量,血管通路的选择,膜及抗凝,对流和弥散清除方式的差异等,具体见持续透析治疗核心课程。KDIGO 指南推荐,CRRT 和 IHD 是互补的治疗,治疗需考虑个体的血流动力学状态,容量过负荷程度,出血风险,治疗设备的可获得性以及治疗经验等。
对于高剂量 CRRT(35 或 45 mL/kg/h)和低剂量 CRRT(20 mL/kg/h)孰优孰劣,研究结果并不一致,现有指南推荐目标置换液流量 20~25 mL/kg/h。至于 IHD 治疗剂量,需检测尿素清除率(URR)或 Kt/V 以保证透析充分性,在 VA/NIH ATN 研究中,IHD 中位持续治疗时间为 4 小时,平均血流速 360 mL/min,在高分解代谢患者中,需强调要有充足的治疗时间以保证治疗效果。
肾脏替代治疗的终止:尿量可能能预测终止肾脏替代治疗的时机,在一项 CRRT 治疗的研究中,未应用利尿剂前提下,24 小时尿量>400 mL 或应用利尿剂情况下,尿量>2300 mL 的患者有>80% 的机会成功脱离肾脏替代治疗。需要有前瞻性的研究进一步指导临床工作者决策何时尝试终止肾脏替代治疗。
(7)对比剂导致的 AKI
对比剂导致的 AKI 治疗管理主要在于预防,对于应用碘对比剂的患者,在操作前 24 小时停用 NSAIDs 药物及肾毒性药物,尽量选择低渗或等渗对比剂,尽可能使用最小对比剂剂量,等渗液体输注减少对比剂导致 AKI 的风险,常用的处方包括对比剂应用前后 12 小时各予 1 mL/kg/h 输注,或者治疗前 1 小时以 3 mL/kg/h 输注,治疗后 4~6 小时以 1.5 mL/kg/h 输注。应用对比剂后血液透析治疗对于阻止对比剂 AKI 的发生并无疗效,并且可能造成危害。
四、AKI 的长期结局
尽管之前的观点认为绝大多数 AKI 患者能够完全恢复,目前认为经历 AKI 的患者后续 AKI 的风险,进展为 CKD 的风险以及今后的死亡风险均有增加,即使轻度的 AKI 也同 CKD 的发生相关。所以,目前推荐所有 AKI 患者需在 AKI 后 3 个月重新评估肾功能,以确定有无新发或加重的 CKD,即使肾功能已经恢复基线的 AKI 患者,进展至 CKD 的风险同样增加。现在尚不明确是否某些干预措施或增加监测频率能够减少这些患者不良结局的风险。
