前言
足细胞折叠性肾小球病(PIG)是近年来提出来的一种新的病理学情况,它是基于电镜下观察到足细胞折叠和陷入肾小球基底膜(GBM)内的独特超微结构所命名的,表现为微球体和微管。自从 2002 年首次发现这种特殊的电镜结果以来,其一直被认为是表现为环状上皮下沉积物的膜性肾病(MN)的变体。直到最近几年,PIG 才被逐渐认识到可能是一种新的不同的疾病实体。
我们在此文中报道一个印度的女性病例,在治疗未分化结缔组织病(UCTD)时出现肾病综合征,病理上满足 PIG 的诊断条件。由于文献中对于 PIG 的报道很少,并且仅限于日本的病例,因此有必要分享其他国家关于此病的病例报道,以便对 PIG 这一肾小球疾病的特点进行归纳。
病例汇报
一位 45 岁的印度女性,被诊断为 UCTD,服用甲氨蝶呤和羟氯喹治疗对称性非变形性炎性多关节炎 1 年余。4 个月后,她出现双下肢浮肿和全身不适 2 个月。没有自身免疫性疾病相关的既往史和家族史。
体检发现患者脸色苍白,双下肢浮肿,血压 130/80 mmHg。实验室检查结果如下:血清肌酐 1.65 mg/dl,血清白蛋白 1.5 g/dl,血红蛋白 7.2 g/dl,血沉 73 mm/h;乙肝和丙肝病毒检测(-),HIV(-)。补体 C3 64.9 mg/dl,C4 22.6 mg/dl;糖化血红蛋白 4.8%;ANA 阳性,dsDNA108 IU/ml,抗 SSA 110RU/ml,抗 SSB 32RU/ml。血清蛋白电泳显示总蛋白和白蛋白水平降低。尿液分析显示:潜血(2+),蛋白(4+),红细胞 20 个/HP,白细胞 10 个/HP。尿蛋白排泄量 5.8 g/d,尿蛋白/肌酐(ACR)9.89。
肾活检结果:总共 15 个肾小球,2 个肾小球局灶节段性系膜增生伴轻度毛细血管壁增厚和局灶节段性硬化(图 1A)。免疫荧光显示 IgG(1+)和 C3 弱阳性,沿毛细血管壁分布。磷脂酶 A2 受体(PLA2R)抗原的免疫组化染色结果阴性。
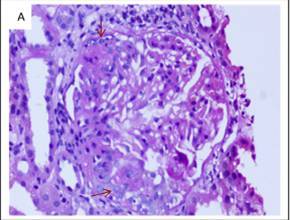
图 1A 光镜下可见肾小球轻度系膜增生伴节段性硬化和轻度的足细胞突起(箭头处)(PAS 染色×200 倍)
电镜显示 GBM 不规则增厚伴环形上皮下特殊的微球体簇集(图 1B~D 和图 2A~C)。弥漫的足细胞足突融合与微绒毛转化有关,并且足细胞胞浆空泡表明足细胞损伤。此外,有足细胞足突全部折叠进增厚的 GBM 中。没有电子致密物沉积在 GBM 或系膜区。基于以上这些结果,做出了 PIG 的诊断。
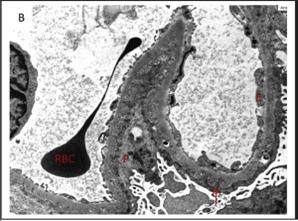
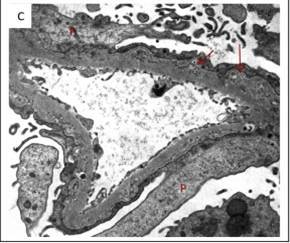
图 1B 肾小球毛细血管壁不规则增厚伴上皮下「沉积物」(箭头处),钉突插入类似Ⅱ期 MN。沉积物的微球体性质在这个放大倍数下看的不是很清楚(投射电镜×6000 倍)图 1C 上皮下微球体簇集(箭头处)伴随Ⅱ期 MN 的分布,足细胞足突广泛融合,并折叠进 GBM 中(投射电镜×8200 倍)
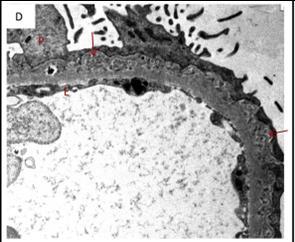
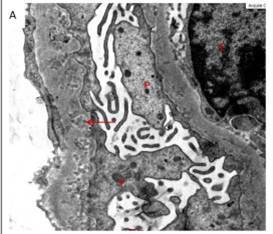
图 1D 微粒体簇集(箭头处)被 GBM 所围绕和分离,类似Ⅱ期 MN 形式(投射电镜×9900 倍)图 2A 经 GBM 分离的上皮下微球和微管簇集(箭头处)。没有分离的电子致密物(投射电镜×11500 倍)
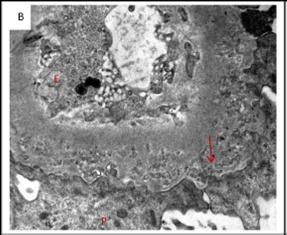
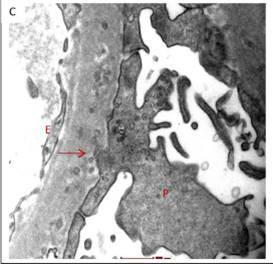
图2B GBM 增厚伴大量上皮下微颗粒聚集(箭头处),是足细胞折叠性肾小球病(PIG)的特征(投射电镜×11500 倍)图 2C 聚集在 GBM 内的微颗粒包围了足细胞足突退化的顶端(投射电镜×20500 倍)
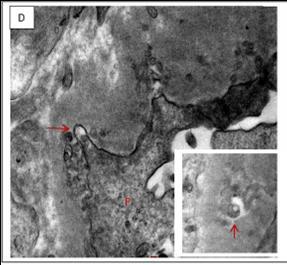
图 2D 足细胞顶端的空泡变性(箭头处)伴近端微球体簇集(投射电镜×26500 倍)插图显示一个由双层膜夹着的透明核心(投射电镜×43000 倍)
患者接受了大剂量泼尼松和吗替麦考酚酯治疗 6 周,激素逐渐减量。考虑到病情活动,予以了 1 g 单一剂量的利妥昔单抗。在 7 个月随访后,肾功能有显著改善(血清肌酐 0.98 mg/dl),蛋白尿逐渐缓解(尿蛋白排泄量 1 g/d,尿 ACR 2.16)。
病例讨论
虽然目前还不清楚 PIG 到底是一种新的疾病还是一种暂时性的形态现象,但是这一病例的特点值得探讨以便更好地了解这种情况。
本病例肾活检标本的光镜结果显示毛细血管壁轻度增厚,伴局灶节段性硬化。联合免疫荧光结果提示外周毛细血管襻 IgG(1+)和 C3 弱阳性,初始做出了 MN 的诊断。然而,电镜结果显示上皮下簇集的直径 50~70nm 的微球体,有些具有明显的双层膜。虽然微球体的亚结构在低倍电镜下不那么清楚,但是在高倍电镜下可见包含了所有 GBM「沉积物」的弥漫性微颗粒亚结构。在这种情况下,有必要将这个病例与 MN 的亚型变种相区分开来,可能是具有不同电镜特点的一个单独的病理实体。
除了在Ⅲ期 MN 和少数乙肝病毒相关性肾小球肾炎的病例中偶见颗粒状和膜性碎片外,在经典的 MN 中通常不会在 GBM 中发现微观结构。我们的病例在电镜下未见免疫型沉积物,排除了 MN 作为主要损害的考虑。患者乙肝病毒也不是阳性。
Kowalewska 等人报道了 14 个伴有微球体 GBM 簇集的 MN 的病例,表现出靶状外观,形态上类似于核孔复合物,但是不具有 ANA 和抗中性肽内切酶(NEP)抗体染色阳性。一例由抗 NEP 抗体诱导的产前 MN 患者同样也有超微结构。虽然缺乏免疫沉积物,不支持 MN 的诊断,但是本病例中观察到的病理超微结构显示足细胞折叠至 GBM 中的范围很广泛。所有这些结果放在一起考虑还是支持 PIG 是主要的病理类型。
PIG 的发病机制还不清楚。术语「微球颗粒」用于描述具有透明核心的膜结合囊泡,直径一般在 40~100nm 之间,在人或多种动物组织的某些胞外位置中发现。微球体在 GBM 中的分布是局灶和节段的,提示病毒感染、肾小球损伤和结晶体等病因需要考虑。PIG 损害是全球性弥漫性分布的。
免疫电镜分析 PIG 的肾小球损害证实细胞外的补体复合物 C5b-C9 和 Vimentin 构成了 GBM 内的结构,提示这些颗粒是足细胞或内皮细胞来源的。截止目前为止,有关 PIG 的大型研究只包含 25 个病人,观察到自身免疫病的发病率较高,激素治疗后蛋白尿水平改善。本例的 PIG 发生在 UCTD 伴低补体血症的患者身上,而且免疫荧光中免疫球蛋白弱阳性,不伴确凿的电子致密物沉积,免疫抑制治疗后肾功能和蛋白尿水平改善。这些结果支持自身免疫异常的假设,伴随补体途径激活在 PIG 的发病过程中起到关键作用。
需要强调足细胞或内皮细胞是否能产生微粒体的问题。病理特征提示足细胞损伤,比如广泛的足突消失、微绒毛转化和细胞质空泡化,在大多数 PIG 的病例中被证明是存在的,在本例中也是如此。此外,位于上皮下的微颗粒和簇集在折叠的足细胞足突周围伴随足细胞尖端空泡变性的微颗粒的特点表明受损的足细胞的崩解过程导致了迁移至 GBM 的微球体的形成。
在将这些超微结构的起源最终归罪于足细胞之前,还需要在更多病例的研究中去评价足细胞特异性蛋白(比如 podocin、肾小球上皮蛋白 1、α-actin4、synaptopodin 和 podocalyxin 等)的表达。除了足细胞损伤外,GBM 异常也可能在 PIG 的发生中起到促进作用。GBM 损伤或异常有助于轻易地捕获退化的足细胞,并随后迁移至 GBM 内,这一观点值得考虑。
目前 PIG 这一罕见的肾小球疾病引起了人们的广泛关注。推荐对所有蛋白尿伴潜在自身免疫性疾病的患者的肾活检标本进行仔细的电镜观察,期待发现更多这样的病例,阐明 PIG 的临床病理学特征,制定将来的管理策略。
