来自意大利 Bambino Gesu 儿童医院肾脏科的 Francesco Emma 和 Dieter Haffner 两位医生联合在 Kidney International 杂志上发表文章,重点阐述了成纤维生长因子(FGF-23)在 X 连锁的低磷酸盐血症的佝偻病(XLH)中的作用,以及抗 FGF23 抗体(burosumab)对 XLH 患儿的治疗效果。让我们一起来重温一下 FGF23 在病理生理学方面的知识以及抗 FGF23 抗体的临床应用。
尿磷酸盐丢失异常的遗传性病因可能是由于原发性肾小管缺陷,改变了近端肾小管中钠偶联磷酸盐的转运,或者更多是由于循环中磷酸盐尿激素水平的升高,特别是 FGF23 水平的升高。FGF23 是首个被描述为导致常染色体显性低磷酸盐佝偻病(ADHR)的磷酸盐尿激素。在 ADHR 中,蛋白质分裂域的错义突变阻止了 FGF23 的失活。之后很快便认识到 FGF23 异常表达于间充质肿瘤细胞导致肿瘤相关的骨软化症,表达于巨大痣细胞引起表皮痣综合征的佝偻病。
高 FGF23 水平也是其它表现为骨软化症或佝偻病的遗传性疾病的特征,从而使 FGF23 成为遗传性低磷血症的主要罪魁祸首。这其中,X 连锁的低磷酸盐血症的佝偻病(XLH, OMIM 307800)是最常见的,约占近 80% 的病例。XLH 的发病率估计在 4/百万出生人口,具有 X 连锁形式的继承和显性表达。
XLH 是由于 PHEX 基因(磷酸调节内肽酶同系物,X 连锁)突变导致发病的,PHEX 基因是编码细胞表面裂解酶的,主要表达于成骨细胞、骨细胞和牙本质细胞。PHEX 突变增加 FGF23 水平的机制还不明确。除了编码肽链内切酶,实验性 PHEX 失活增加了 FGF23 分泌,而不是防止其失活。
XLH 患儿通常表现为佝偻病、蹒跚步态、腿部畸形和不成比例的身材矮小。成人通常有身高降低、腿部畸形和骨软化。他们容易骨折和假性骨折,经常遭受疼痛,关节僵硬和损伤,以及牙脓肿,所有这些都严重影响他们的生活质量。FGF23 通过抑制刷状缘磷酸钠偶联转运体的表达,以及通过抑制线粒体中维生素 D3 的 1α羟基化而在近端肾小管细胞中发挥作用(图 1)。
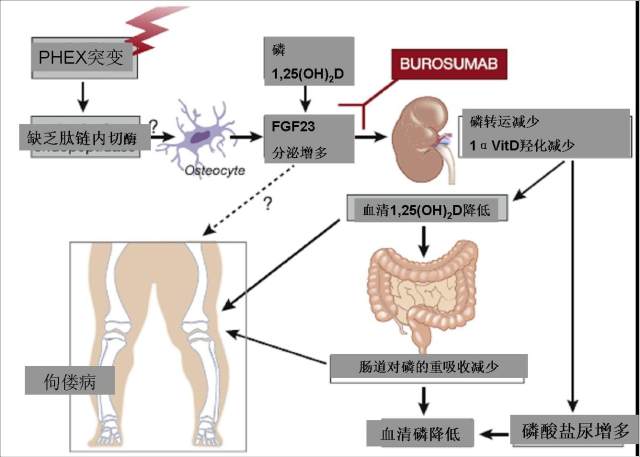
图 1 X 连锁的低磷酸盐血症的佝偻病(XLH)的病理生理机制
因此,多年来 XLH 的治疗依赖于磷酸盐和活性维生素 D 的补充,这抵消了循环中高 FGF23 水平的一些后果,但是在大多数患者中并不能纠正 XLH 的表型,其原因还没完全搞清楚。部分可能是由于 FGF23 对外周组织的直接和间接效应。此外,传统的治疗可能导致不良反应,尤其是肾钙质沉着症与甲状旁腺功能亢进症会增加 FGF23 的水平,进一步刺激肾脏磷的排泄。
FGF23 在 XLH 病理生理中的关键作用被 Hyp 小鼠(一种 XLH 的小鼠同源物)所证实。给 Hyp 小鼠注射抗 FGF-23 抗体后,血清磷水平和 1,25-二羟维生素 D 水平正常,并改善了骨的表型。因此,burosumab(以前称为 KRN23),一种重组的完全人源化的抗 FGF-23 IgG1 单克隆抗体就被研发出来了。
初期在有症状的成人 XLH 患者中进行的 2 期临床试验结果显示,burosumab 改善了血清磷和 1,25-二羟维生素 D 的水平,而没有严重的不良反应。一项在成人患者中进行的双盲安慰剂对照的 3 期临床预实验(24 周治疗)的结果刚刚公布,提示活动骨折愈合和关节僵硬减少。在成人中,病变通常是退行性的,妨碍了全面评估抗 FGF23 治疗的潜在益处。
近期,Carpenter 等人报道了一项公开标签的 2 期临床试验的结果,该试验在 52 名 5 ~ 12 岁的 XLH 和活动性佝偻病的患儿中比较了除了传统治疗之外,两种不同剂量的 burosumab 的治疗效果。
结果证实,经过 40 周每月皮下注射一次或两次的 burosumab 治疗,患儿佝偻病的严重程度得以显著改善,效果可持续到 64 周。病情的改善在接受一月两次 burosumab 治疗和基线时佝偻病更严重的患儿中更显著。Burosumab 两种剂量组患儿的血磷水平均增加,虽然血磷水平在一月接受两次 burosumab 治疗的患儿中更稳定,但是在 6 周内有超过一半的受试者达到正常范围。在试验期间血清碱性磷酸酶水平显著改善。这些结果与显著的疼痛和体能改善相符。不良反应轻微,大多数与注射部位反应有关。
基于这些有利结果,burosumab 近期被欧洲和美国的卫生行政部门批准用于治疗 XLH(仅限于儿童),一周两次。但是需要强调以下事项。首先,在截止目前所有的试验中,burosumab 的剂量都是调整到以达到血清磷正常范围的低限水平为准。burosumab 的最佳治疗策略,包括给药频次和血磷的靶目标范围等,可能不同于已获得满意表型改善的患者。
其次,从 burosumab 的高额费用和缺乏长期有效性和安全性数据的角度来看,需要更加明确哪些患者能从治疗中获益。因为,儿科的临床试验严格限定患者年龄<12 岁,burosumab 在青春期中的安全性和有效性还需要进一步评估。在接受 burosumab 治疗的儿童中,生长发育的短期改善为中度。并不清楚这些接受治疗的儿童是否会经历持续性的生长追赶并达到正常的成人身高。
最后,burosumab 对 XLH 其它严重并发症(如牙脓肿和感音神经性耳聋)的影响,还需要在将来的研究中进一步去强调。
除了 burosumab 之外,在未来几年会有相似的药物进入市场。在这些药物中,FGF23 受体拮抗剂 NVP-BGJ398 已进入晚期研发阶段。
总结
由于 FGF23 与多种临床疾病的病理生理学的关系越来越密切,尤其是与慢性肾脏病(CKD)相关的骨矿物质代谢紊乱(CKD-MBD)的发生有关,是近年来基础研究的热点。在 CKD 中,FGF23 的表达水平随着肾功能降低而逐渐增加,与 CKD 高磷血症的发生密切相关。作为成人肾脏科医生,希望将来能有更多的基础和临床研究支持抗 FGF23 抗体(burosumab)用于 CKD 患者高磷血症的治疗。
