来自美国马里兰大学肾脏科的 Preeti Chandra 教授近期在 American Journal of Nephrology 杂志上发表综述文章,概括了补体 C4d 在肾小球疾病中沉积的意义。我们一起来学习一下。
补体激活途径回顾
多种肾小球疾病中都存在补体激活。补体激活有 3 种途径:经典途径(CP)、凝集素途径(LP)和替代途径(AP)。三条途径聚合在 C3 转化酶形成处,激活 C3,产生 C3a 和 C3b 两种活性形式,后者与 C3 转化酶结合,形成 C5 转化酶,将 C5 裂解成 C5a 和 C5b 两种活性形式。C5b 进一步与 C6、C7、C8 和 C9 结合形成 C5b-9 这一膜攻击复合物(MAC)。MAC 引起无核细胞的溶解,但对有核细胞造成亚致死性的损伤,包括细胞活化和组织损伤。
CP 通常由抗原抗体复合物形成所激活,最终导致 C1s 的活化,将 C2 和 C4 裂解为活性形式。LP 由甘露糖结合凝集素(MBL)或无花果素与细菌体内碳水化合物部分结合激活,这导致 MBL 相关丝氨酸蛋白酶(MASPs)的激活,MASP 可以裂解 C4 和 C2。CP 和 LP 都会导致 C4b2b 形成,发挥类似 CP/LP 中 C3 转化酶的作用。在 AP 中,硫酯键的水解可以自发激活 C3,因此引入了 B 因子和 D 因子。D 因子将 B 因子裂解,形成活化的丝氨酸酯酶(Bb),然后将 C3 转化为 C3a 和 C3b。C3b 与 Bb 结合形成 AP 中的 C3 转化酶 C3bBb。(图 1)
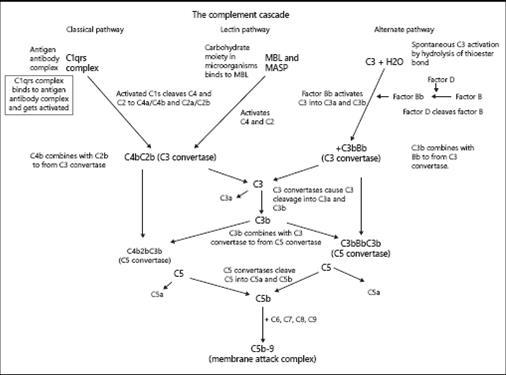
图 1 补体活化途径
C4d 沉积在肾小球疾病中的意义
C4d 是 CP 和 LP 中 C4 活化的裂解产物。由于其硫酯键,它可以共价结合到细胞表面,并可以作为补体激活的标志物。在肾移植中,C4d 出现在管周毛细血管(PTG)伴随着移植物肾损伤和供体特异性抗体阳性,就可以诊断为急性抗体介导的排斥反应(AMR),AMR 与较差的预后有关。另一方面,在 ABO 血型不合的同种异体移植物的 PTC 处 C4d 染色阳性而没有组织学损伤,被认为代表了移植物的适应。近年来关于 C4d 在肾小球疾病中沉积的报道也越来越多,具体详见表 1。
表 1 C4d 在不同病理类型的肾小球疾病中的沉积部位和可能的活化途径
诊断 | C4d 在肾小球内的沉积部位 | 导致 C4d 沉积的可能的补体途径 |
IgA 肾病 | 大部分系膜区 | 凝集素途径 |
膜性肾病 MN | 主要是沿着肾小球毛细血管壁 | 凝集素途径、可能有经典途径 |
局灶节段硬化 FSGS | 关于 C4d 沉积没有数据 | |
微小病变病 MCD | 未在 MCD 中观察到有 C4d 沉积 | |
膜增生性肾炎 MPGN | C4d 主要沿着毛细血管襻沉积 | 经典途径和凝集素途径 |
狼疮性肾炎 LN | 肾小球毛细血管壁、有些系膜区、 有些病例是在管周毛细血管 | 经典途径、凝集素途径 |
ANCA 相关性血管炎 | 毛细血管壁、系膜区 | 凝集素途径、可能有经典途径 |
抗 GBM 肾炎 | 肾小球毛细血管壁 | 经典途径 |
血栓性微血管病 TMA | 肾小球、小动脉、 极少数病例沉积在管周毛细血管 | 大部分病例是经典途径 有些病例是凝集素途径 |
感染后肾炎 | 肾小球毛细血管壁、系膜区 | 凝集素途径或经典途径 |
C4 肾小球肾炎 C4 G | 肾小球毛细血管壁、系膜区 | 凝集素途径 |
结论
肾小球内 C4d 沉积可以是补体 CP 或 LP 活化的结果。C4d 伴随 C1q 和免疫球蛋白的沉积,提示 CP 活化。伴或不伴免疫球蛋白沉积,以及不伴 C1q 的沉积,提示 LP 活化。免疫球蛋白,如 IgA 和半乳糖缺乏型 IgG,被认为可以活化 LP。此外,有些数据提示,在心脏缺血再灌注损伤的模型中,IgM 可以活化 LP。
在有些肾小球疾病中 C4d 沉积似乎与较差的肾脏预后有关。C4d 染色阳性以及其它补体成分的沉积,将有助于描述肾小球疾病中不同的补体激活途径,有助于了解肾小球疾病的发病机理。此外,在有些疾病中,C4d 染色可能有助于明确肾脏预后较差的患者亚类,这将有助于指导治疗决策。由于市场上目前已有影响补体途径的新型药物,因此在不同的肾小球疾病中确定关键的补体途径就很重要。
免疫组化法进行 C4d 染色是一种简单的染色方法,大部分实验室都能进行,当不能进行免疫荧光检查时,免疫组化法就显得很有价值。未来还需要进一步在动物模型中开展试验和在患者中进行前瞻性研究,具体研究不同补体途径的沉积和激活以及它们在肾小球疾病中的作用。
