肾小球疾病约占成人急性肾损伤(AKI)的 10%。表现为 AKI 的肾小球疾病谱多种多样,取决于年龄、性别、种族和地域以及肾活检策略。在健康个体中,肾脏有助于维持免疫稳态,而免疫系统的成分则介导了许多肾脏疾病的急性形式。新月体性和非新月体性急性肾小球肾炎都可以表现为 AKI。高度怀疑表现为 AKI 的肾小球疾病时,需要结合实验室的检查结果。肾活检是诊断的金标准。
AKI 既可以通过致病机制介导,也可以通过蛋白尿和血尿等损害的临床症状介导。肾小球疾病的主要临床-生物学表现为:急性肾炎综合征、肾病综合征(NS)和快速进展性肾小球肾炎(RPGN)。这篇发表在 2019 年 12 月 Curr Opin Crit Care 杂志上的文章就肾小球疾病中 AKI 的发病机制做了一项系统的综述。
血尿和 AKI
大量血尿通过不同的病理机制促进肾功能的损害。IgA 肾病(IgAN)是最常见的原发性肾小球肾炎,也是导致肾小球性血尿最常见的病因。大约一半的患者会表现为大量血尿,而另一半患者则表现为镜下血尿。感染后肾小球肾炎或狼疮的 RPGN、小血管性血管炎和急性肾小球炎症也可能与肾小球性血尿相关。血尿在毛细血管内皮和毛细血管外肾小球肾炎中很常见,但主要是基于观察性队列研究。
来自西班牙的肾活检登记数据报道:在传统认为不以血尿为表现的患者(包括微小病变病、膜性肾小球肾炎或局灶节段性肾小球硬化)中,血尿的比例出人意料的达到 50%,但是肉眼血尿的发生很少见。在新近发现的 C3 肾小球肾炎中,血尿-主要是镜下血尿,也出现在很高比例的患者中。
AKI 可能是由于肾小球来源的大量血尿引起的。肾小管细胞的损伤是由肾小管内的血细胞管型阻塞和肾小管细胞吞噬红细胞的过程引起的。因此,大量血尿持续的时间是肾功能恢复的关键。红细胞释放血红蛋白(Hb)产物,进一步被肾小管细胞吸收。一旦进入细胞内,Hb 分离,释放球蛋白和血红素,由此导致多种致病效应,包括氧化应激、细胞死亡、炎症和纤维化。
最近发现除了肾小管细胞外,足细胞可能也是 Hb 介导的肾脏损伤的细胞靶点。因此,Hb 诱导氧化应激性损害,足细胞功能不全并且最终凋亡,从肾小球毛细血管中脱离。Hb 通过毛细血管壁的运输可损伤足细胞,并可能导致肾小球滤过屏障的改变。
肾小球滤过屏障渗漏引起的红细胞损伤促进了含有 microRNA(miRNA)的微血管的释放。miRNA 可被几乎所有的细胞吞噬,并通过调节基因表达在氧化应激和细胞间通讯中起重要作用。IgAN 血尿患者尿中 miRNA 的检出率较高,主要来源于尿红细胞。血尿相关 miRNA 可改变肾实质细胞基因的表达,促进肾脏疾病的发展。miRNA 在血尿相关 AKI 发病机制中的作用仍有待进一步研究证实。
肾病综合征(NS)和 AKI
近年来,NS 中 AKI 的发生率日益增多。在成人特发性 NS 中 AKI 更常见,它能使所有 NS 病例复杂化。NS 中的 AKI 通常是可逆的,发病机制也是多因素的。在 NS 患者中,尤其是在微小病变病(MCD)患者中,可逆性影响肾小球毛细血管结构的因素不明确,导致 GBM 对血清白蛋白的渗透性增加,并降低其对水和小分子的渗透性。
近年来有关 NS 中 AKI 流行病学的大部分信息都来自病例报告。Smith 等人报道:AKI 发生的平均时间是在 NS 发生后的(29±5)天。在 58 位肾功能恢复的患者中,AKI 持续了 7 周。尽管 AKI 归因于容量不足,但是大多数患者在纠正容量不足后肾功能没有改善,60% 的病例有与急性肾小管坏死相一致的组织病理学改变。
相反地,在更近期的一项有关特发性 NS 的研究里,277 名患者中的绝大多数肾功能都恢复。更多严重的 AKI 与更长的缓解时间和更低的完全缓解(CR)率有关。在 logistic 回归分析中,严重的低蛋白血症、高龄和男性被认为是危险因素。
与非 AKI 患者相比,AKI 患者的血管、肾小管和肾小球等处的内皮素 1(ET-1)的免疫反应性更强。ET-1 作用于肾脏血管处,诱导血流量和 GFR 降低。NS 伴 AKI 的患者在 NS 发生时会经历暂时的循环不足。另一方面,肾小管细胞可以重新滤过蛋白质。与这一假设相一致的是观察到在最严重的 AKI 病例中,肾缺血过程在老年和/或高血压肾硬化患者中,减少了肾小球的入球动脉的血供。这些微血管损伤和炎症间质纤维化、肾小管萎缩一起损害了肾小管的活力。
多年来一直将 NS 钠潴留和肾功能不全的病理生理机制归因于低血容量状态。实际上,在稳定状态下,在没有使用袢利尿剂治疗的情况下,血流量并不减少。在肾病性水肿中,低血浆白蛋白浓度和间质内液体较高的压力会达到一个新的平衡。在这种情况下,间质液体被淋巴系统吸收,增加的淋巴流量保持血浆容量接近正常。
在某些病例系列中,缺血性肾小管损伤和肾小管坏死也有报道,但其内在机制仍不清楚。最近,Fujigaki 等研究了 37 例成人 MCD 患者肾小管细胞的变化。37 名患者中 13 名(35.1%)有 AKI,发现有些肾小管损伤标志物(如尿 NAG 和尿α1 微球蛋白)水平显著增加。发现在 AKI 组中,Vimentin(另一种肾小管损伤的标志物)免疫组化的表达水平也显著增加。
快速进展性肾小球肾炎(RPGN)和 AKI
RPGN 是一种急症。早期诊断和治疗可以改善预后,在治疗开始,血肌酐是最佳的预测指标。表现为 RPGN 的免疫相关性疾病的经典例子便是抗肾小球基底膜疾病(抗 GBM 疾病)和抗中性粒细胞胞质抗体(ANCA)相关性血管炎,均表现为 AKI 的新月体性肾小球肾炎,常常还伴有严重的肺泡出血(Good Pasture 综合征)。
循环抗体与 IV 型胶原α3 链的 NC1 域结合。自身抗原暴露的潜在触发因素还不清楚。但是一旦结合发生,就会导致进一步的构象变化,使抗原-抗体复合物的形成永久化。导致免疫复合物沿着 GBM 线性沉积,主要是由 IgG 和补体成分构成,损伤周围的内皮细胞和足细胞,导致免疫细胞浸润。
肾脏受累的 AAV 表现为血尿、蛋白尿和滤过功能迅速的受损,以肾小球血管损伤为特点。AAV 的进展速度很快,与肾活检标本中新月体性肾小球疾病的形态一致,伴随严重的肾小球坏死性破坏。
AAV 病理损害的发生机制还没有完全弄清楚。可能是由肾小球损伤引起的,激活了中性粒细胞,导致中性粒细胞胞外陷阱(NETs)的脱颗粒和排出。NETs 的挤压促进 ANCA 相关抗原(包括髓过氧化物酶、蛋白酶 3 和溶酶体相关膜糖蛋白)随后被循环中的 ANCA 抗体结合。
此外,体内研究表明 PR3-ANCA 可以直接激活循环中的中性粒细胞。自身反应性 T 细胞也被认为是 AAV 的致病机制。由激活的中性粒细胞释放的活性氧自由基,与 NETs 结合的自身抗体和广发活化的白细胞导致了局部的炎症和肾小球毛细血管内的补体活化。这一血管的炎症导致了局灶性坏死伴肾小球屏障破坏,临床表现为血尿和快速降低的肾功能。
巨噬细胞是一种髓样免疫细胞,分布在全身组织中,来源于循环中的单核细胞。一旦被激活,巨噬细胞可以变成经典活化的 M1 型(进一步促进组织损伤)或者变成活化的 M2 型(促进组织修复)。Zhao 等人发现在纤维素样坏死的部位主要是 CD68+和 CD163+的巨噬细胞,超过了中性粒细胞和 T 细胞的数量。
此外,AAV 患者中正常外观的肾小球较对照组有显著更多的 CD68+和 CD163+的巨噬细胞。作者假设 M2 型巨噬细胞可能是纤维素样坏死和随后新月体形成的前奏。Rousselle 等人在小鼠 AAV 模型中发现单核细胞可以促进新月体的形成。这些研究清楚地提示巨噬细胞/单核细胞与血管炎的肾损害有关。
还发现补体沉积与细胞性新月体有关,在 AAV 中起作用。在节段性纤维蛋白样坏死的发生过程中,单核细胞和 CD3+T 细胞在间质浸润,导致进一步的肾脏损害。补体系统在肾脏疾病致病机制中的重要作用最近又再次被强调。非典型溶血尿毒综合征(aHUS)和某些膜增生性肾小球肾炎明显继发于遗传异常或损害补体替代途径(CAP)的调节蛋白(如补体 H 因子、补体 B 因子、膜辅因子蛋白)活性的循环抗体。
此外,其它形式的肾小球肾炎(如狼疮性肾炎、冷球蛋白血症性肾小球肾炎)由补体激活所触发。最近 AAV 也被添加到这一名单上。过去几年的研究证实,大多数患者在损伤部位至少有部分补体沉积,而且肾小球内补体的沉积(尤其是 C3 的沉积)与较差的肾功能和肾脏预后有关。
这些发现是由使用 AAV 小鼠模型的体内研究所引起的,并且证实补体级联的末端部分,特别是 C5 的激活。补体系统在 ANCA 相关性坏死性新月体性肾小球肾炎中的致病相关性由免疫组化研究所证实,显示肾小球和血管内沉积的免疫复合物是由补体碎片组成的。CAP 在 AAV 中的主要作用是基于活动性 AAV 患者血浆 C3a 和 Bb 水平高于静止性 AAV 患者的假设。
与肾小球疾病有关的 AKI 的其它机制
大部分免疫介导的肾脏疾病是由于自身免疫失调导致的,但是有些也是由于补体级联反应的遗传缺陷或血液系统的恶性肿瘤(如多发性骨髓瘤或何杰金氏淋巴瘤)所导致的。继发于免疫稳态丧失的肾脏损伤主要以下三个机制引起:循环免疫复合物沉积、补体替代途径失调和单克隆免疫球蛋白的沉积。其它机制也有提及,比如在血栓性微血管病中,细胞因子局部浓度升高,靶向全身血管的自身抗体导致下游缺血性损伤。
免疫复合物通过激活循环免疫细胞和表达 Fc 受体的肾脏固有细胞而损伤肾小球内皮细胞、上皮细胞和系膜。激活的细胞分泌细胞因子和血管活性物质,在免疫复合物沉积后产生促炎症环境。此外,通过经典途径激活的补体级联反应终点的膜攻击复合物的形成,损伤周围的细胞,导致进一步的致炎症信号。免疫复合物沉积导致的肾小球肾炎的代表便是 IgAN、狼疮性肾炎、膜增生性肾小球肾炎或感染相关性肾小球肾炎。
补体系统的过度激活导致的肾脏损伤是由于补体调节成分的基因突变或针对补体系统成分的自身免疫性疾病引起的。C3 沉积可形成于肾小球内,激活下游的炎症级联反应并促进白细胞浸润。在致密物沉积病(DDD)中,沿着基底膜形成小的带状电子致密的补体沉积,导致基底膜增厚和功能障碍。除了 GBM 沉积外,C3 肾小球病也显示出不同程度的系膜 C3 沉积,导致系膜细胞增生和基质扩张。C3 沉积导致的肾小球肾炎的例子便是 C3 肾小球病。
肾血管树的损伤也可以通过与免疫稳态丧失相关的情况来介导。HUS,无论是经典的腹泻相关型还是非典型的非腹泻相关型,都可以表现为 AKI。与 HUS 损害表现相似的是血栓性微血管病(TMA)。
原发性抗磷脂抗体综合征(APS)是一种自身免疫性疾病,以循环中抗磷脂抗体(aPLs)阳性、复发性静脉或动脉血栓和妊娠相关性问题为特点。aPLs 包括狼疮抗凝物、抗心磷脂和抗β2 糖蛋白 I,导致了致凝状态,在有致凝因素(如氧化应激、外科干预或感染)存在的情况下导致血栓形成。大约 10% 的原发性 APS 患者会发生肾脏受累,小比例的患者会表现为 AKI。
最后, AKI 可以发生在混合性冷球蛋白血症的患者中,由于冷球蛋白造成微血管闭塞,引起肾炎。
结论:与肾小球疾病相关的 AKI 很常见。有时候会表现为急诊的病例。对肾脏疾病的各种机制的了解日益增加,并可能有助于预防和治疗。
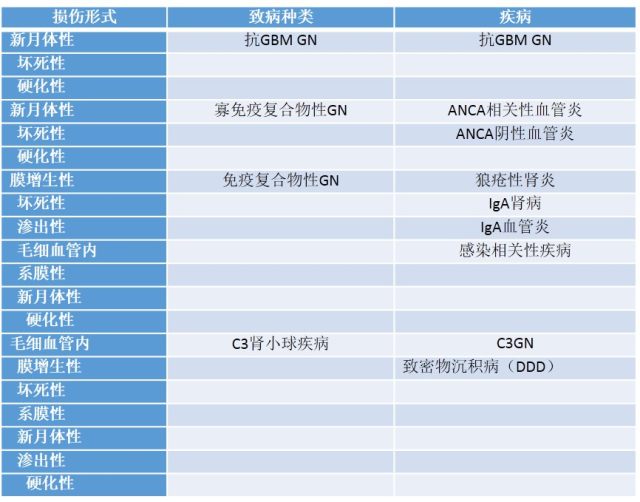
表-1 损伤形式和特异性肾小球疾病