肾性贫血是终末期肾病(ESRD)患者常见的并发症,铁剂和促红细胞生成素(EPO)是临床常用的治疗药物。但有时即使予以了足量的 EPO 和铁剂,患者依然存在贫血。此时我们就要考虑到可能引起贫血的其它病因。来自美国纽约 Hofstra Northwell 医学院肾脏科的 Steven Fishbane 博士在 2017 年 7 月的 CJASN 杂志上发表了一个教学查房病例,详细分析了一例血透患者难治性贫血的原因及治疗过程。让我们一起跟着该病例复习一下肾性贫血的相关知识吧!
病例介绍
一位 71 岁的老年女性,因对 EPO 类似物治疗抵抗而接受评估。过去 5 年里,她接受了一周三次的中心血透治疗。ESRD 的原发病因不清。既往病史包括:甲减、抑郁症、高血压和乳腺癌。
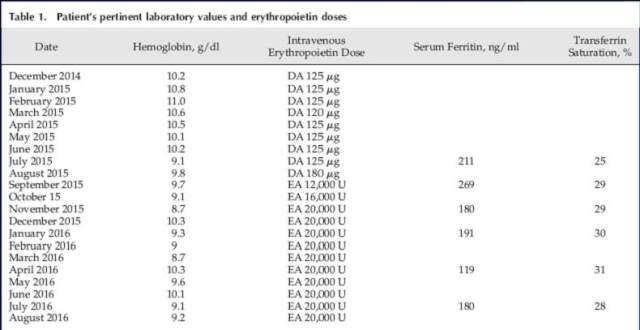
在过去的 18 个月里,她的贫血变得越来越难治疗,血色素(Hb)水平通常<10 g/dl,她需要大剂量的 EPO(见表 1)。她承认最近几个月的疲劳感增加了。在此次就诊评估前的两个月曾发生了一个无明确诊断的晕厥的小插曲。
她目前的用药有:氨氯地平、西那卡塞、西酞普兰、司维拉姆、间隙使用静脉铁剂,每次透析时接受 EPO-α 2000U 治疗。
体格检查:血压 160/84 mmHg,体温正常。除了右臂的动静脉内瘘和她左腿外侧的红斑,其余检查正常。
2016 年 1 月的实验室检查结果:Hb 水平 9.3 g/dl、正常红细胞指数、网织红细胞(Hct)计数 0.8%、转铁蛋白饱和度 30%、血清铁蛋白水平 191 mg/dl、Kt/V 1.43。2016 年 6 月甲状旁腺激素(PTH)水平 672pg/ml。
EPO 抵抗的定义
关于 EPO 抵抗并没有普遍认可的定义。全球改善肾脏病结局组织(KDIGO)贫血专家组将其定义为「如果使用稳定剂量的红细胞生成剂(ESA)治疗后,仍然需要 ESA 剂量增加 50% 才能保持稳定的 Hb 浓度」。我们给出了一个简单的定义:在任何情况下都难以维持 Hb 在目标范围内,尤其是当每周 EPO-α的剂量>20000U 或达依泊汀α剂量>80ug/周。如果碰到患者体重极低或极高的情况,还是推荐 KDIGO 定义的标准。
EPO 抵抗的主要病因架包括对血液学的因素、炎症状态和潜在的与透析有关的可修正的因素三方面。具体包括:血液丢失、铁缺乏、炎症、感染、营养不良、血液系统疾病、透析相关的(根据 Kt/V 和 URR 判断的透析不充分、继发性甲状旁腺功能亢进)因素。
评估血液学因素
对于 EPO 抵抗造成的贫血应该首先评估是否存在血细胞的生成缺陷、血液丢失或溶血。Hct 绝对计数是了解对贫血的反应的一个良好检测手段。低水平的 Hct 可能提示红细胞产生不足。
对 EPO 抵抗的研究应该从评估失血开始。虽然铁缺乏可能是条线索,但是血清铁蛋白水平甚至在铁缺乏的透析患者中也可能会升高。透析患者由于抽血采样、通过透析管路端口的出血时间和经过透析器的凝血时间延长,慢性失血的风险很高。此外,透析患者胃肠道失血的风险也增加。对失血的全面评估包括仔细检查血管通路或手术可能导致的额外失血以及大便隐血试验。
出现铁缺乏是 EPO 抵抗的另一个重要原因,血透患者可能每年丢失 1000-3000 mg 铁。在患者的铁剂治疗过程中,评估铁饱和度和血清铁蛋白水平很重要。例如,一位患者虽然经过静脉铁剂治疗,但铁蛋白和转铁蛋白饱和度水平仍然很低,那么透析中心的铁剂治疗方案可能需要提高铁剂剂量。然而,需要较大剂量的 EPO 之前总是需要评估是否有大便隐血阳性,因为只有少数患者需要>50 mg/周的静脉铁剂来补偿透析相关的常规铁丢失。
至于评估铁状态,KDIGO 指南指出「对于接受 ESA 治疗而未接受补铁治疗的成人 CKD 患者,我们建议如果存在下列情况进行静脉铁剂试验:需要升高 Hb 水平或减少 ESA 剂量,而转铁蛋白饱和度<30% 且铁蛋白<500ng/ml」。
本例的患者血清铁蛋白和转铁蛋白饱和度水平对于接受血透治疗的患者而言偏低。虽然她间断的接受过静脉铁剂治疗,但是不足以维持足够的铁平衡,很可能是由于她的 EPO 抵抗与相对铁缺乏有关。
除了贫血部分的评估,肾脏科医生还应该观察全血细胞情况。出现白细胞减少或血小板减少可能提示骨髓造血功能不良,需要转诊至血液科医生处。其它实验室检查项目需要留意红细胞指数、溶血的指标如胆红素、乳酸脱氢酶和结合珠蛋白水平等。
纯红细胞再生障碍性贫血(PRCA)是由于抗 EPO 抗体产生所导致的,是一种非常罕见但是很严重的疾病,会导致 EPO 抵抗进行性加重需要输血。表现为 Hb 每周降低 1 g/dl,并且 Hct 计数<10000/mm3,通常更低,常常<3000/mm3。骨髓评价显示红细胞前体的分离和严重丢失。如果怀疑 PRCA 的诊断,应立即停止使用 EPO,因为抗体会与所有的 EPO 制剂起反应。
评估炎症状态
引起 EPO 抵抗的另一个重要原因便是出现营养不良-炎症复合综合征(MICS),这其中包括炎症状态、蛋白能量营养不良和偶尔的感染。透析患者较普通人群的炎症指标升高。研究证实炎症指标(如 C 反应蛋白)较高的患者需要更大剂量的 EPO。病理生理机制尚未明确,但是血清铁调素(抑制储存组织中铁的吸收和释放)水平增加,可利用的铁减少,至少是部分原因。
感染或炎症可能显而易见,但是对隐匿性炎症的来源也应该进行评估。较少见的原因可能与导管和生物膜形成有关,旧的无功能性的动静脉移植物可能被感染。已经证实营养状态与 EPO 反应性之间存在负相关关系。但目前还没有肯定的证据证明营养干预能改善 EPO 的反应性。
这位患者长期的 EPO 抵抗使得显性感染的可能性很小,但是在血透患者中经常能发现的隐匿的尚未完全被探明的微炎症状态可能导致了她的 EPO 抵抗。对 C 反应蛋白的检查和临床评估并未发现感染或炎症是她 EPO 抵抗的原因。
评估透析相关的因素
还应该评估与透析处方有关的潜在的修正因素和继发性甲状旁腺功能亢进(SHPT)。透析不充分是 EPO 抵抗一个可能但是很少见的病因。事实上,该患者的 Kt/V 结果尚在可接受的范围内。
在文献中,SHPT 是引起 EPO 抵抗的一个重要原因,在全段 PTH(iPTH)水平>600pg/ml 并且碱性磷酸酶(AKP)水平>160U/L 的患者中最常见。在美国,iPTH 水平>600pg/ml 的透析患者比例在 2010 年-2015 年期间从 11% 增加至 22%。
尚不清楚骨髓纤维化是否能完全解释 EPO 的反应性降低。既往研究证实许多贫血的透析患者存在 SHPT,进行甲状旁腺切除手术后 EPO 反应性该改善,贫血有所改善。维生素 D 或西那卡塞的药物治疗可能也有效,可以减少高达 33% 的 EPO 剂量需求。
病例讨论
当这位患者第一次在我们这就诊时,我们并未看到 iPTH 的检查结果。2016 年 1 月她的 AKP 水平是 800U/L,逐渐升高至 2016 年 6 月的 2125U/L。这要高度怀疑胆汁淤积性肝病、潜在的恶性肿瘤或严重的甲状旁腺功能亢进症。对她的临床评估基本上排除了肝脏疾病或恶性肿瘤。当 AKP 水平增加时,如果骨病是主要病因的话,应检测骨特异性的 AKP 水平。
我们接下来回顾了她的 iPTH 结果。2016 年 1 月时她的 iPTH 水平是 672pg/ml,仅稍高于 KDIGO 的靶目标范围。然而,在 2015 年 7 月时,她的 iPTH 水平是 1848pg/ml,接下来 2016 年 6 月时 iPTH 水平是 3994pg/ml。到 2016 年 6 月之前,除了外科切除手术治疗外,没有其它治疗方法。在 2016 年 6 月底进行了甲状旁腺近乎全切术。术后 iPTH 水平立即降低,血清 AKP 水平在接下来的 3 个月里降低至 245U/L。
在 2016 年 12 月之前,她的 Hb 浓度是 10.9 g/dl 伴随着达依泊汀α剂量减少至 10000U,每周三次。EPO 反应性的显著改善与甲状旁腺切除术之间的时间关联使我们有理由认为严重的甲状旁腺功能亢进是该患者 EPO 抵抗最重要的原因。
这个病例遗留的其它问题
首先,存在从达依泊汀α切换到 EPO-α。我们不知道是否有证据支持对其中一种药物抵抗可以通过切换为另一种药物来解决这个问题。
其次,EPO-α剂量每次从未增加超过 20000U。虽然有证据提示较大剂量的 EPO 可以部分克服抵抗,但是潜在的安全事项也必须要考虑。食品药品监督管理局(FDA)给 EPO 药物贴的标签是「使用最低剂量的 EPO 以满足降低输注红细胞的需求」。
第三,甲状旁腺功能亢进是否应该更早的积极治疗?在本病例中,医生致力于提高患者的依从性,将患者的血清钙、磷控制在正常范围内而降低 iPTH 水平。我们不认为 EPO 抵抗是加速手术治疗的一个令人信服的理由,因为只要 Hb 保持在可以避免症状和需要输血的水平即可。更多的关注应该是对患者骨头和肌病症状的影响。
结论
ESRD 患者的 EPO 抵抗可以由多种不同因素导致。经过深思熟虑的临床评估往往会寻找出特定病因,并有助于指导治疗。随着 iPTH 水平的升高,在治疗过程中要继续保持警惕以避免 EPO 抵抗和由于 PTH 持续升高导致的其它并发症。
