系统性红斑狼疮(SLE)是一种自身免疫性疾病,以大量产生自身抗体、补体过度激活、细胞残骸的防御性清除和免疫复合物生成为特征,导致多器官组织损伤。C 反应蛋白(CRP)是一种感染血清标志物,一种公认的可溶性模式识别受体,其通过激活补体有利于死亡细胞或病原体入侵的去除。
狼疮肾炎(LN)患者体内经常有 CRP 的自身抗体。由于它们在狼疮患者中普遍存在,因此被认为其产生可能仅仅是全身性炎症引起的附带现象,而且其多克隆的性质也掩盖了其致病和诊断意义。明确 CRP 的自身免疫标位,可以提升患者的分层,并揭示 CRP 活性的机制。
北京大学第一医院的学者们在之前工作的基础上, 进一步研究 LN 患者氨基酸 35-47(a.a. 35-47)介导单体 CRP(mCRP)与补体的相互作用,将研究成果发表在近期的美国肾脏病学杂志上。
作者指出,a.a. 35-47 构成 LN 患者体内被抗-CRP 自身抗体识别的主要肽段。特别是抗 a.a. 35-47 的自身抗体与严重肾损伤和预期后果相关。
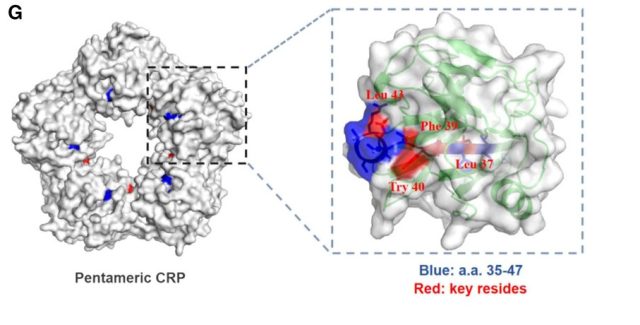
图:氨基酸 35-47 是狼疮性肾炎中 CRP 的主要自身免疫抗原表位
ELISA 和表面等离子共振分析显示 mCRP 与补体因子相互作用。mCRP 可以通过与补体 C1q 激活经典的补体途径来促进细胞碎片的清除,同时通过招募补体因子 H(CFH)来阻止补体过度活化。然而,在清除机制不堪重负的情况下,mCRP 被运送到淋巴结并被 B 细胞识别,从而导致产生自身抗体。
本文鉴定了两种自身免疫表位,结果显示 a.a.35-47 能更好的代表 mCRP,只有在结构发生不可逆改变后,CRP 上的表位才会暴露出来。而 a.a. 199-206 可能暴露在 mCRP 和 CRP 上,可逆或中等构象变化就会暴露出来。因此,抗 a.a.35-47 的自身抗体对组织损伤的潜在机制更为具体。
作者的研究结果为疾病时人体中产生 mCRP 提供了证据,并且表明 mCRP 可以通过补体活化来积极控制狼疮肾炎的发病机理。因此,a.a. 35-47 构成的 CRP 功能性自身免疫表位,可以作为治疗和诊断的靶向。
给予合成的 a.a. 35-47 治疗时,可以有以下作用:
(1)中和相应的自身抗体,以释放它们对 mCRP 与 CFH 相互作用的抑制作用;
(2)抑制 mCRP 诱导的促炎细胞反应;
(3)直接增强 CFH 的辅因子活性以限制过度的补体激活。
